
2024年2月12日,中国医学科学院基础医学研究所暨永利集团3044官网欢迎您免疫治疗研究中心曹雪涛院士团队在Nature Communications《自然通讯》在线发表题为“EFHD2 suppresses intestinal inflammation by blocking intestinal epithelial cell TNFR1 internalization and cell death”(EFHD2通过抑制肠道上皮细胞TNFR1内化和细胞死亡抑制肠道炎症)的研究论文。该研究报道了肠道炎症的关键抑制分子,加深了对受体膜转运调控的理解,为死亡受体信号和自身炎症性疾病提供了新的见解。
炎症性肠病(IBD),包括克罗恩病(CD)和溃疡性结肠炎(UC),是一种以肠道屏障破坏和严重肠道炎症反应为特征的胃肠道慢性炎症性疾病。肠上皮细胞(IEC)的大量死亡引起肠道黏膜屏障的缺陷和紊乱,导致严重且持续的肠道炎症。肿瘤坏死因子(TNF)作为重要的细胞因子,是诱导IEC死亡和肠道炎症的致病驱动因素之一。然而,机体对IEC死亡的内源性抑制从而调控肠道炎症的分子机制仍有待进一步研究。
EF-hand结构域蛋白D2(EF-hand domain-containing protein D2,EFHD2,又称Swiprosin-1)是一种钙结合蛋白,具有两个保守的EF-chiral coiled-coil结构域,主要参与钙信号转导、细胞骨架组装和突触形成。该团队曾发现在巨噬细胞中,EFHD2可以介导γ干扰素受体2从高尔基体到细胞膜的转运过程。前期实验表明,EFHD2在人正常肠组织中高表达,但在UC患者的肠道活检样本中却表达下降。Efhd2缺失的原代IEC对于TNF诱导的死亡效应更加敏感;同样,TNF诱导下Efhd2缺失的肠道类器官的细胞凋亡显著增加。IEC特异性缺失Efhd2的小鼠表现出IEC死亡增加和实验性结肠炎加剧的表型。体内外实验均证明Efhd2能够抑制TNF诱导的IEC死亡和肠道炎症反应。机制研究表明,EFHD2与丝切蛋白(Cofilin)相互作用,通过抑制Cofilin的磷酸化,从而阻断TNF受体Ⅰ(TNFR1)的内化过程,抑制IEC凋亡,从而保护肠道免受炎症侵袭(见图1)。
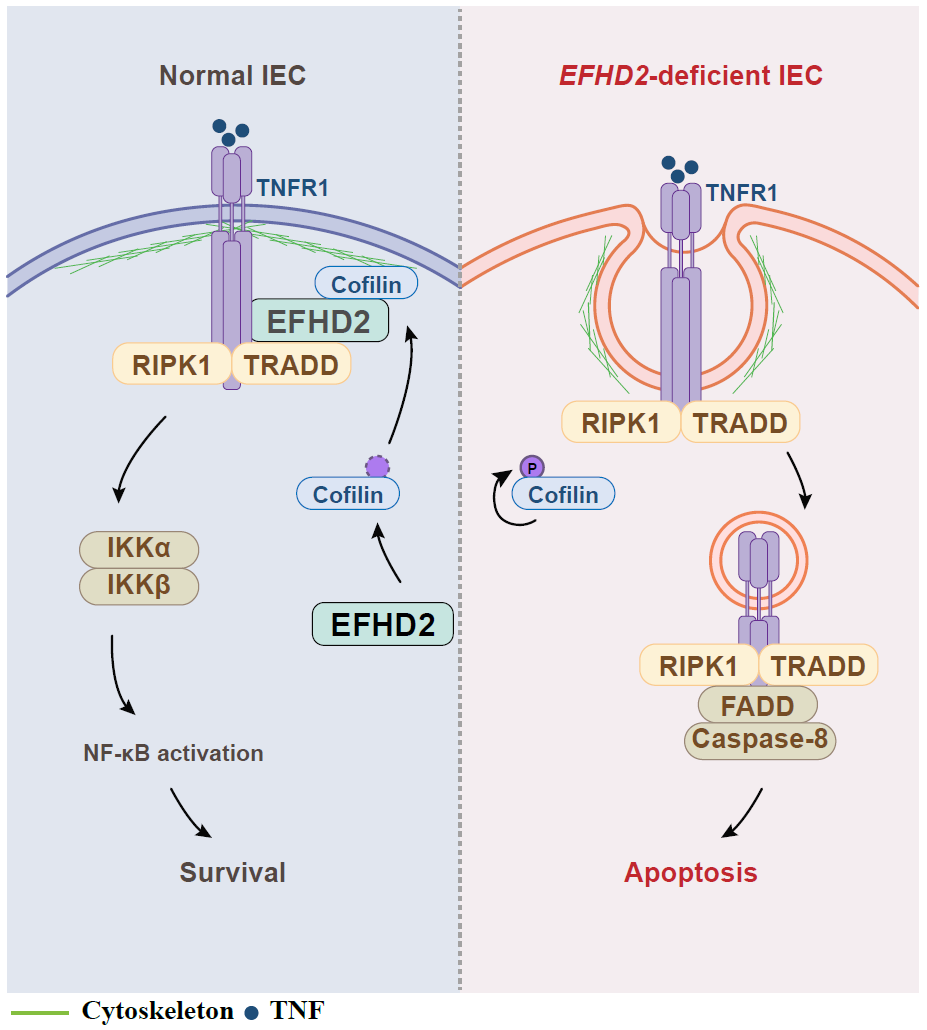
图1.EFHD2抑制TNFR1内化作用抑制肠道炎症的模式图
该研究提示EFHD2是一种IEC死亡的内源性抑制因子,它通过抑制TNFR1的内化过程保护肠道免受过度炎症的影响。该发现为死亡受体信号的空间调控提供了一个新的视角,增加了对死亡受体信号和自身炎症性疾病的认识。同时,该研究表明,EFHD2的表达水平可能作为一个潜在的预测指标,指导抗TNF疗法对溃疡性结肠炎的临床治疗。
本研究工作得到国家自然科学基金基础科学中心项目(82388201)和永利集团3044官网欢迎您医学与健康科技创新工程(2021-I2M-1-017)等项目的资助。基础医学研究所曹雪涛教授和北京协和医院李景南教授为论文共同通讯作者,基础医学研究所助理研究员吴佳宬和许小青副研究员为论文的共同第一作者。
论文链接:https://www.nature.com/articles/s41467-024-45539-x